
nom féminin
(bas lat. materia, class. materies, bois de construction)
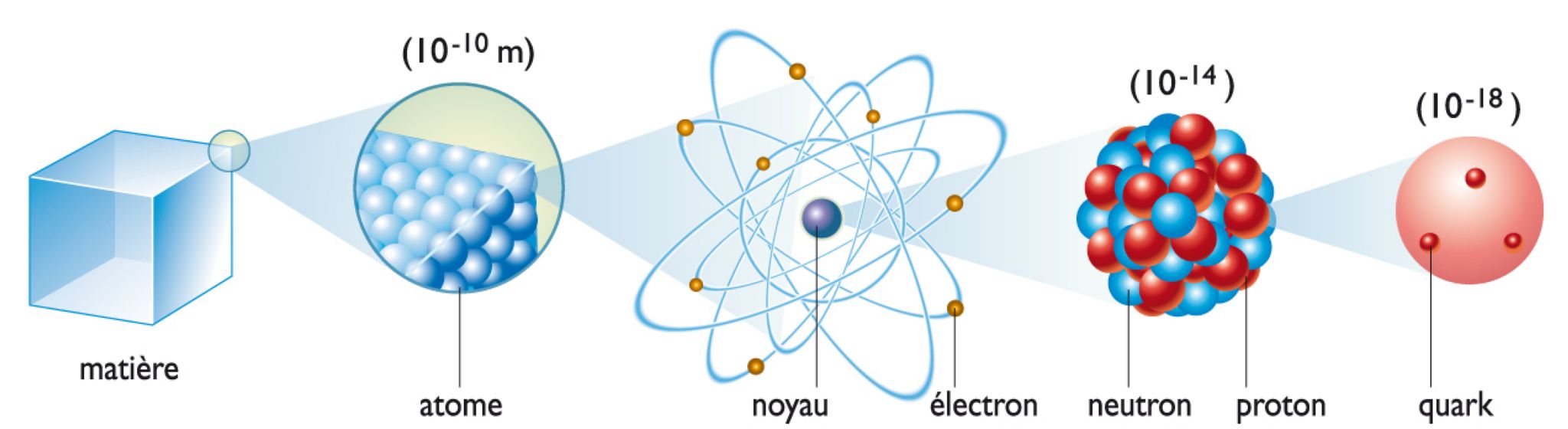


Entrée en matière, début, introduction d'un exposé, d'un discours, d'une étude, etc.
Matière première, matériau d'origine naturelle qui est l'objet d'une transformation artisanale ou industrielle : La laine, le coton sont des matières premières.
Table des matières, liste fournissant l'indication des sujets traités dans un ouvrage, et leur référence.
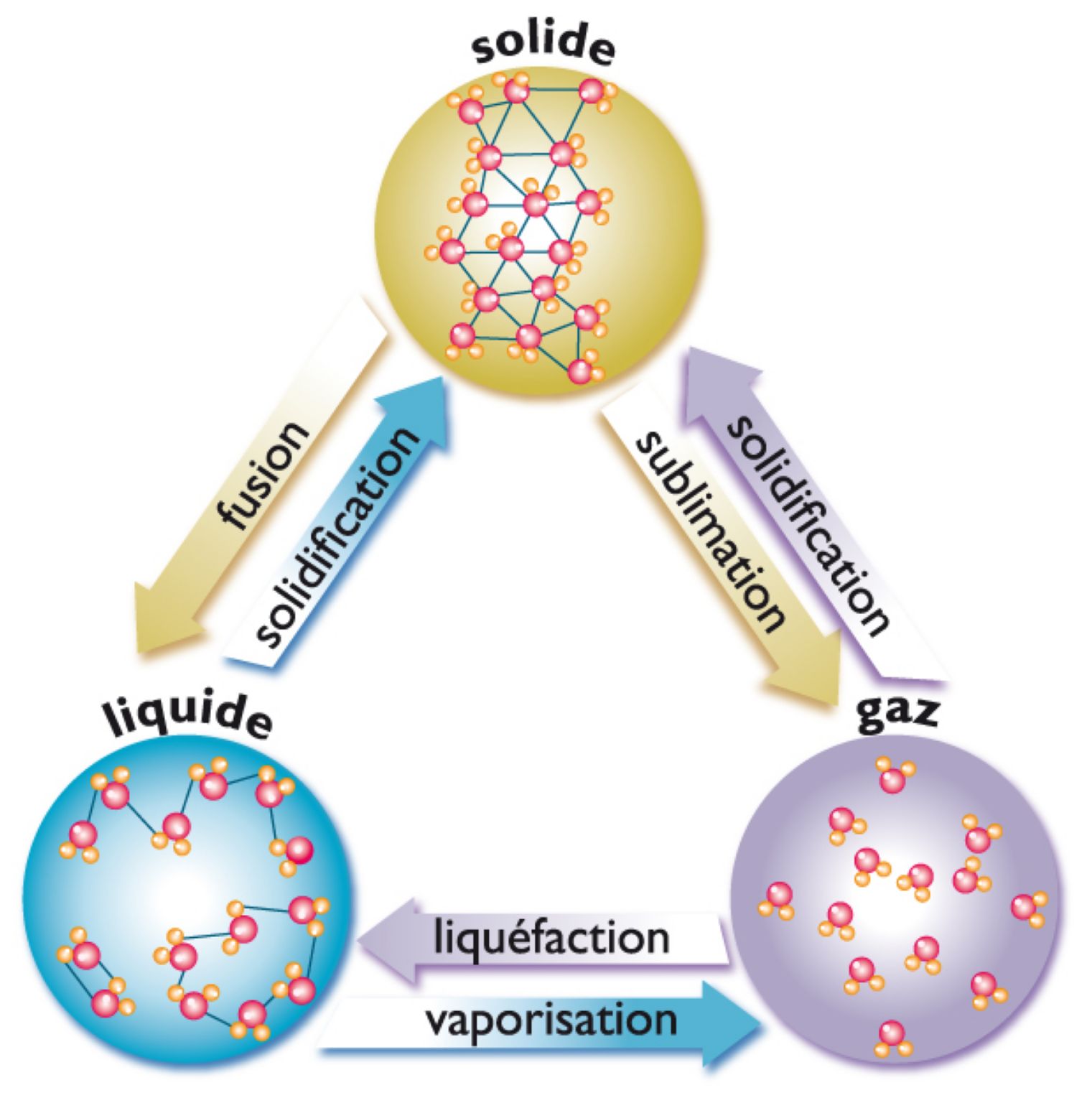
Les états de la matière.
L'état physique d'un corps dépend de la proximité de ses éléments constitutifs, atomes, ions ou molécules. Dans un solide, ils sont tassés les uns contre les autres et quasi immobiles. Dans un liquide, bien qu'encore proches, ils ont la possibilité de se mouvoir. Dans un gaz, ils sont parfaitement libres de se déplacer dans tout le volume qui leur est offert. Selon la température et la pression auxquelles il est soumis, un corps pur quelconque peut passer d'un état à l'autre.
Au-delà d'environ 10 000 °C, molécules et atomes se dissocient. C'est dans cet état, dit « plasma », que se trouve la majeure partie de l'Univers. Certains objets astronomiques où règnent d'énormes pressions, les étoiles à neutrons, résultent même de la désintégration des noyaux des atomes.
Au-dessus de 0 °C, la glace fond et se transforme en eau : chauffée au-dessus de 100 °C, à une pression atmosphérique normale, l'eau devient un gaz, la vapeur d'eau. Inversement, la vapeur d'eau se condense au contact d'une paroi froide en donnant de l'eau, qui peut à son tour se transformer en glace. Comme beaucoup d'autres corps, l'eau peut ainsi passer de façon réversible par les trois états. À la pression atmosphérique, certaines substances, l'iode par exemple, passent directement de l'état solide à l'état gazeux : elles se subliment.
Changements d'état.
Les trois types possibles, fusion/solidification, vaporisation/liquéfaction et sublimation/condensation, peuvent être provoqués par des variations de température, c'est-à-dire des modifications de l'agitation thermique des molécules. Le passage d'un état à un autre, cependant, s'effectue sans variation de température : à la pression atmosphérique, lorsqu'un glaçon fond dans un verre d'eau, la température de celle-ci reste strictement égale à 0 °C, de même que celle de l'eau en train de bouillir est de 100 °C. L'énergie nécessaire pour provoquer ce dernier changement d'état, la chaleur latente de vaporisation, est employée à vaincre les forces d'attraction qui lient les molécules d'eau.
Les corps ne connaissent pas tous ces changements d'état : certains solides se décomposent avant de fondre, et certains liquides avant de se transformer en gaz.